- Detalhes
- Categoria: PROGEMULTI
- Última atualização: 10 Junho 2025
- Detalhes
- Categoria: PROGEMULTI
- Última atualização: 11 Junho 2025
Objetivos do MultiMassas/UERJ:
a) desenvolver pesquisas, treinamento e prestação de serviços especializados que envolvam o uso das técnicas de espectrometria de massas com foco em metabolômica e proteômica;
b) propor convênios e contratos com entidades públicas e privadas, com vistas ao intercâmbio de conhecimentos e prestação de serviços especializados;
c) dar apoio ao Hospital Universitário Pedro Ernesto e a Policlínica Piquet Carneiro nas atividades ligadas às técnicas desenvolvidas no MultiMassas/UERJ;
d) oferecer estágios aos alunos de graduação e pós-graduação desta Universidade e de outras instituições com foco em linhas de pesquisa que utilizem as técnicas desenvolvidas no MultiMassas/UERJ.
Comitê Gestor:
a) Prof. Alex C. Manhães (UERJ): Coordenador Científico;
(http://lattes.cnpq.br/1445083298662873)
b) Profa. Paula Helena K. Barreira (UERJ);
(http://lattes.cnpq.br/1290495617933793);
c) Profa. Regina Célia Cussa Kubrusly (UFF)
(http://lattes.cnpq.br/1719959034374657);
d) Dr. Ulisses Cesar Araújo (UERJ): Chefe Operacional.
(http://lattes.cnpq.br/4926360383520029).
Comitê de Usuários:
a) Prof. Yael de Abreu Villaça (UERJ);
(http://lattes.cnpq.br/2110538573461886)
b) Profa. Patrícia C. Lisboa (UERJ);
(http://lattes.cnpq.br/6704904748735082)
c) Profa. Nathália Curty de Andrade (UERJ).
(http://lattes.cnpq.br/5522336668110013)
Corpo Técnico:
a) Dr. Ulisses Cesar Araújo (UERJ);
(http://lattes.cnpq.br/4926360383520029)
b) Thamires Christinne de Souza Lopes Cruz Serrão (UERJ).
(http://lattes.cnpq.br/5668921292264983)
Espaços Físicos:
a) Laboratório Principal: localizado no andar térreo do Pavilhão Reitor Haroldo Lisboa da Cunha, campus Maracanã da UERJ;

b) Laboratório Complementar: localizado no andar térreo do Pavilhão Reitor Haroldo Lisboa da Cunha, campus Maracanã da UERJ;

c) Sala de Bioinformática: localizado no andar térreo do Pavilhão Reitor Haroldo Lisboa da Cunha, campus Maracanã da UERJ.
Equipamentos:
a) Espectrômetro de Massas Waters SYNAPT G2-S HDMS 8k;

b) Espectrômetro de Massas Waters XEVO G2-S Tof 4k;

c) Espectrômetro de Massas Waters XEVO TQD;

d) Espectrômetro de Massas Waters ACQUITY QDa Performance.
![]()
Links:
a) Plataforma Nacional de Infraestrutura de Pesquisa MCTI (PNIPE):
https://pnipe.mcti.gov.br/laboratory/16543
b) Programa de Gestão de Equipamentos e de Laboratórios Multiusuários da UERJ:
http://progemulti.sr2.uerj.br:8080/emu/#/#top
Publicações recentes do MultiMassas/UERJ:
a) Nucleus Accumbens Proteome Disbalance in an Adolescent Mouse Model of Schizophrenia and Nicotine Misuse Comorbidity. Biomedicines. 2025 Apr 8;13(4):901. doi: 10.3390/biomedicines13040901.
https://pubmed.ncbi.nlm.nih.gov/40299488/
b) Changes in the proteome of Apis mellifera acutely exposed to sublethal dosage of glyphosate and imidacloprid. Environ Sci Pollut Res Int. 2024 Jul;31(33):45954-45969. doi: 10.1007/s11356-024-34185-x. Epub 2024 Jul 9.
https://pubmed.ncbi.nlm.nih.gov/38980489/
c) Nicotine Exposure in a Phencyclidine-Induced Mice Model of Schizophrenia: Sex-Selective Medial Prefrontal Cortex Protein Markers of the Combined Insults in Adolescent Mice. Int J Mol Sci. 2023 Sep 27;24(19):14634. doi: 10.3390/ijms241914634.
https://pubmed.ncbi.nlm.nih.gov/37834084/
Contato:
E-mail: O endereço de e-mail address está sendo protegido de spambots. Você precisa ativar o JavaScript enabled para vê-lo.
Endereço: Rua São Francisco Xavier, 524, Pavilhão Haroldo Lisboa da Cunha, 1º andar, Maracanã, Rio de Janeiro – RJ – CEP 20550-900. Tel.: (21) 2868-8029.
Atenção: Os agendamentos para uso dos equipamentos estão suspensos até a conclusão das manutenções programadas.
- Detalhes
- Categoria: PROGEMULTI
- Última atualização: 25 Março 2021
 Laboratório: Centro de Pesquisa em Biologia Celular e Ômicas / BIOOmics
Laboratório: Centro de Pesquisa em Biologia Celular e Ômicas / BIOOmics Laboratório: Centro de Pesquisa em Biologia Celular e Ômicas / BIO-Omics
Laboratório: Centro de Pesquisa em Biologia Celular e Ômicas / BIO-Omics Laboratório: Centro de Pesquisa em Biologia Celular e Ômicas / BIO-Omics
Laboratório: Centro de Pesquisa em Biologia Celular e Ômicas / BIO-Omics- Detalhes
- Categoria: PROGEMULTI
- Última atualização: 10 Junho 2025
 1) Cromatógrafo a Líquido, com detector de arranjo de diodos
1) Cromatógrafo a Líquido, com detector de arranjo de diodos 2) Espectrofotômetro UV-Visível
2) Espectrofotômetro UV-Visível 3) Liofilizador de bancada
3) Liofilizador de bancada
- Detalhes
- Categoria: PROGEMULTI
- Última atualização: 25 Março 2021
 Sistema automático para análise tradicional de Injeção em Fluxo - FIA
Sistema automático para análise tradicional de Injeção em Fluxo - FIA- Detalhes
- Categoria: PROGEMULTI
- Última atualização: 25 Março 2021
 Criostato
Criostato  Ressonância magnetica nuclear
Ressonância magnetica nuclear  Untracentrífuga HITACHI himac modelo CP-80WX (Tóquio, Japão)
Untracentrífuga HITACHI himac modelo CP-80WX (Tóquio, Japão)- Detalhes
- Categoria: PROGEMULTI
- Última atualização: 25 Março 2021
 1) Sequenciador automático de DNA
1) Sequenciador automático de DNA 2) Centrífuga de placas
2) Centrífuga de placas 3) Termociclador para PCR em tempo real (Real-time PCR)
3) Termociclador para PCR em tempo real (Real-time PCR) 4) Espectrotômetro Nanodrop
4) Espectrotômetro Nanodrop 5) Termociclador
5) Termociclador 6) Extrator automatizado de DNA
6) Extrator automatizado de DNA- Detalhes
- Categoria: PROGEMULTI
- Última atualização: 10 Junho 2025
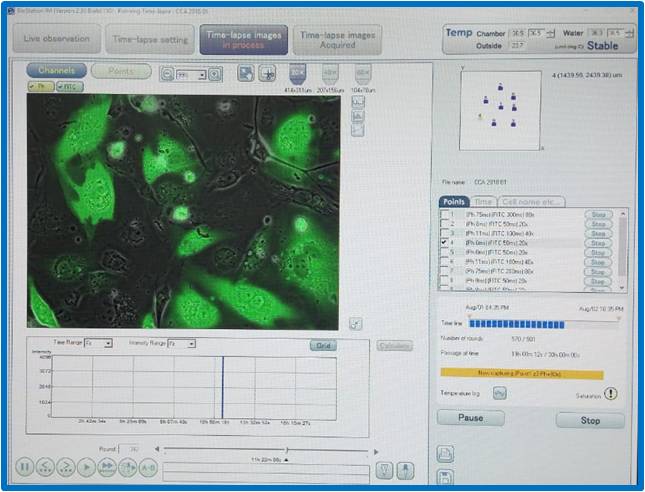

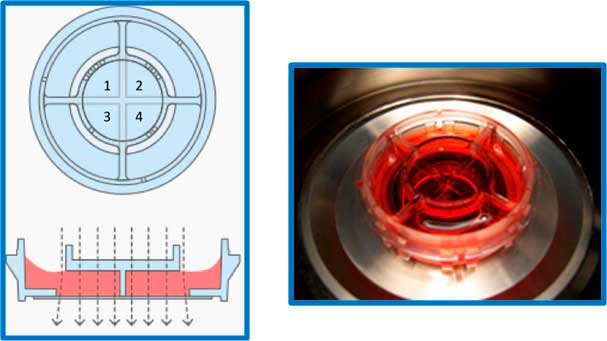
Eletroporador4D-Nucleofector - Lonza
Fonte financiadora: Convênio CT-INFRA FINEP 01.12.0361.03


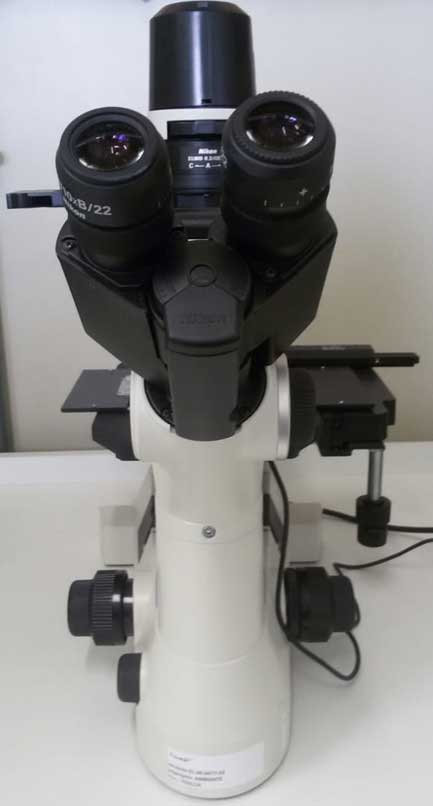
A eletroporação é um método físico de transfecção, que permeabiliza a membrana celular através da aplicação de um pulso elétrico que move moléculas da membrana, gerando poros transitórios que permitem a entrada de biomoléculas exógenas (DNA, RNA e proteínas ) nas células. A eficiência de transfecção de grandes fragmentos de DNA por esse método é muito grande, tanto para a maioria das linhagens celulares contínuas, quanto para células primárias.
O eletroporador Nucleofector-4D (Lonza) exibe taxas de eficácia de transfecçãomais elevadas, quando comparado aos eletroporadores tradicionais, devido à optimizações metodológicas que aumentam a transfecção diretamente ao núcleo (“nucleofecção”). O Nucleofector-4D é equipado com a Unidade de Controle (Core Unit) e com o módulo operacional X, no qual células em suspensão podem ser transfectadas, seja em cubetasestéreis de 100μL, ou em “strips” estéreis com 16-wells (20 μL/poço), ideais para a optimização do método. Kits de transfecção, a serem adquiridos à parte pelos usuários, foram otimizados pelo fabricante para a transfecção para da maioria das linhagens comercialmente disponíveis.
Programas de eletroporação específicos para as mesmas linhagens podem ser acionados através do software de controle do Nucleo fector-4D. Tipos celulares não constantes da lista irão requerer a execução de um procedimento de optimização. Recomenda-se usar 1-5 x106 células nas cubetasde 100 μLe 2 x105 células nos 16-well strips. Os usuários interessados devem consultar informações detalhadas no site http://knowledge.lonza.com (LonzaKnowledgeCenter).


- Detalhes
- Categoria: PROGEMULTI
- Última atualização: 07 Fevereiro 2025
 Equipamento: Microscópio Confocal LSM 510 HW Rel. 3.5 and higher / Axio Ob
Equipamento: Microscópio Confocal LSM 510 HW Rel. 3.5 and higher / Axio Ob Equipamento: Microscópio Eletrônico de Transmissão (MET)
Equipamento: Microscópio Eletrônico de Transmissão (MET) Equipamento: Microscópio Eletrônico de Varredura (MEV)
Equipamento: Microscópio Eletrônico de Varredura (MEV)- Detalhes
- Categoria: PROGEMULTI
- Última atualização: 10 Junho 2025

 Evaporador rotativo à vácuo
Evaporador rotativo à vácuo